Saviez-vous que votre intestin abrite des billions de micro-organismes essentiels à votre santé ? Ces microbes, formant le microbiote intestinal, jouent un rôle clé dans la régulation de votre système immunitaire. Des études récentes montrent que des déséquilibres dans cette communauté microbienne, appelés dysbioses, pourraient déclencher ou aggraver des maladies auto-immunes comme la polyarthrite rhumatoïde ou le diabète de type 1 (source).
Points clés :
- 5 à 8 % de la population mondiale souffrent de maladies auto-immunes, souvent liées à une altération du microbiote.
- Les acides gras à chaîne courte (AGCC), produits par certaines bactéries intestinales, réduisent l'inflammation et renforcent la barrière intestinale.
- Une alimentation riche en fibres et faible en graisses saturées peut améliorer la diversité microbienne et limiter les réponses inflammatoires.
Plongeons dans les mécanismes fascinants qui connectent votre intestin à votre immunité.
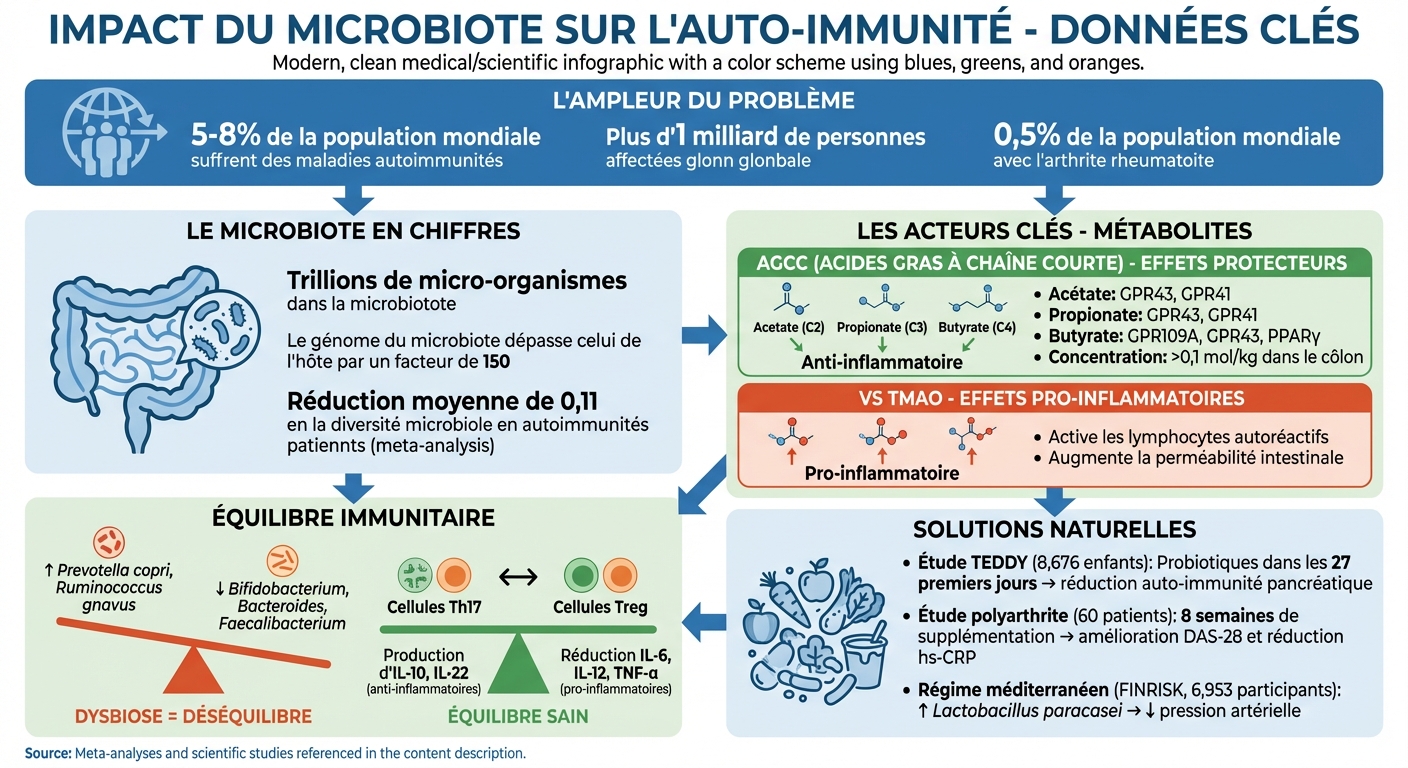
Impact du microbiote intestinal sur l'auto-immunité : statistiques clés et mécanismes
Comment le microbiote intestinal régule le système immunitaire
Diversité microbienne et équilibre immunitaire
La diversité du microbiote intestinal joue un rôle central dans le développement et le bon fonctionnement du système immunitaire. Un microbiote riche et varié soutient la maturation des tissus lymphoïdes associés à l'intestin (GALT) et influence l'équilibre entre les cellules Th17 et Treg, deux acteurs clés de la réponse immunitaire [1][8].
Certaines bactéries ont des effets opposés sur cet équilibre. Par exemple, les SFB (Segmented Filamentous Bacteria) stimulent les cellules Th17, connues pour leur rôle dans les réponses inflammatoires, tandis que des bactéries comme Lactobacillus et Bifidobacterium favorisent les cellules Treg Foxp3+, qui agissent pour limiter l'inflammation [1][8]. Une méta-analyse menée sur des patients atteints de maladies auto-immunes a montré une réduction moyenne de 0,11 de la diversité microbienne, soulignant un lien potentiel entre une diversité réduite et des déséquilibres immunitaires [7].
« Le microbiote exerce une influence protectrice sur l'auto-immunité en favorisant la régulation immunitaire, bien qu'il puisse également déclencher une réponse immunitaire pro-inflammatoire. » - Mohammad Adawi, Laniado MC, Ariel University [7]
Passons maintenant à l'impact des métabolites produits par les bactéries intestinales sur l'inflammation et la réponse immunitaire.
Métabolites microbiens et inflammation
Les bactéries intestinales transforment les fibres alimentaires en acides gras à chaîne courte (AGCC) comme le butyrate, l'acétate et le propionate. Ces composés ne se contentent pas de nourrir les cellules du côlon : ils jouent également un rôle clé dans la modulation des réponses immunitaires. Par le biais de récepteurs spécifiques (GPCR) et de mécanismes épigénétiques, ils influencent l'activité des cellules immunitaires [1][7].
Le butyrate se distingue particulièrement : il favorise la différenciation des cellules Treg, essentielles pour limiter les réponses inflammatoires, et inhibe la voie de signalisation NF-κB, un acteur majeur de l'inflammation. Par ailleurs, les AGCC stimulent la production de cytokines anti-inflammatoires comme l'IL-10 et l'IL-22, tout en réduisant les cytokines pro-inflammatoires telles que l'IL-6, l'IL-12 et le TNF-α [8]. Ces mécanismes montrent à quel point les métabolites microbiens peuvent influencer l'équilibre inflammatoire.
Intégrité de la barrière intestinale et fonction immunitaire
La barrière intestinale joue un rôle crucial en tant que frontière entre le microbiote et le système immunitaire. Elle repose sur des protéines de jonction serrée comme la Zona Occludens 1 (ZO-1), les occludines et les claudines, qui assurent son étanchéité [8]. Lorsque cette barrière est compromise, un phénomène souvent appelé « syndrome de l'intestin perméable » survient, permettant à des molécules comme les lipopolysaccharides (LPS) de pénétrer dans la circulation sanguine. Cela peut déclencher des réponses inflammatoires et favoriser des maladies auto-immunes.
Un microbiote équilibré soutient cette barrière grâce à la production de butyrate, qui constitue une source d'énergie essentielle pour les cellules épithéliales du côlon [1][8]. Cependant, si la barrière est endommagée, les récepteurs TLR (Toll-Like Receptors) sont activés, entraînant la libération de cytokines pro-inflammatoires (IL-1β, IL-6, TNF-α) [8]. Cela illustre l'interconnexion complexe entre le microbiote intestinal et le système immunitaire, d'autant plus que le génome du microbiote dépasse celui de l'hôte par un facteur de 150 [7].
Microbiote : à la poursuite de l’immunité intestinale - Futurapolis Santé 2024
Dysbiose intestinale et maladies auto-immunes
Un microbiote en déséquilibre ne se limite pas à perturber la régulation immunitaire ; il peut également déclencher des mécanismes pathologiques spécifiques. La dysbiose, ce déséquilibre microbien, est intimement liée au développement et à l'aggravation de maladies auto-immunes. Par exemple, des profils microbiens particuliers sont associés à des pathologies comme la polyarthrite rhumatoïde.
Polyarthrite rhumatoïde et bactéries intestinales
La polyarthrite rhumatoïde (PR) touche environ 0,5 % de la population mondiale[11]. Des études ont révélé une prolifération marquée de bactéries telles que Prevotella copri et Ruminococcus gnavus chez les personnes atteintes de PR, accompagnée d'une diminution d'espèces considérées comme protectrices, notamment Bifidobacterium, Bacteroides et Faecalibacterium[1][5][3].
Un élément central dans ce processus est l'action de certaines bactéries capables de produire des enzymes PAD (peptidylarginine deiminase). Ces enzymes catalysent la citrullination des peptides de l’hôte, une modification des protéines qui peut entraîner la formation de néo-antigènes. Ces néo-antigènes peuvent ensuite déclencher une réponse auto-immune, surtout chez les individus ayant une prédisposition génétique[1][4].
Une étude notable, SCREEN-RA, conduite en Suisse entre septembre 2019 et octobre 2021 auprès de 371 participants, a mis en lumière un point intéressant : l'augmentation de la famille Prevotellaceae n'était significative que chez les patients ayant développé des symptômes cliniques avancés. Cette augmentation n’a pas été observée lors des phases précliniques de la maladie[11]. Ces résultats renforcent l’hypothèse selon laquelle la dysbiose intestinale joue un rôle moteur dans l’apparition et la progression de l’auto-immunité.
« La dysbiose microbienne est le principal moteur des maladies inflammatoires et auto-immunes locales telles que la colite et les maladies inflammatoires de l'intestin. La dysbiose intestinale peut également déclencher des maladies auto-immunes systémiques telles que le diabète de type 1, la polyarthrite rhumatoïde et la sclérose en plaques. »
– Walaa K. Mousa, Département de biologie, Whitman College[10]
Recherches sur les métabolites microbiens et l'inflammation auto-immune
Les molécules produites par le microbiote intestinal jouent un rôle clé dans la régulation de l'inflammation et des maladies auto-immunes. Ces métabolites, véritables messagers biochimiques, peuvent soit apaiser les réponses immunitaires, soit les exacerber. Deux exemples frappants illustrent cette dualité : les acides gras à chaîne courte (AGCC), qui possèdent des propriétés anti-inflammatoires, et le triméthylamine-N-oxyde (TMAO), un composé associé à des réactions inflammatoires.
AGCC et effets anti-inflammatoires
Les acides gras à chaîne courte, comme l'acétate (C2), le propionate (C3) et le butyrate (C4), sont produits lors de la fermentation des fibres alimentaires et des amidons résistants dans le côlon. Ces molécules atteignent des concentrations supérieures à 0,1 mol/kg dans le côlon humain[13].
Leur action repose sur plusieurs mécanismes. Les AGCC agissent comme des inhibiteurs naturels des histones désacétylases (HDAC), favorisant ainsi l'acétylation des protéines. Ce processus stimule la production de cellules T régulatrices (Tregs), de cellules B régulatrices (Bregs) et de macrophages producteurs d'IL-10[13]. Ils interagissent également avec des récepteurs spécifiques (GPR41, GPR43, GPR109A) présents sur les cellules immunitaires et épithéliales pour moduler des voies inflammatoires comme NF-κB.
« L'inhibition des HDAC par les AGCC génère également des Tregs, des Bregs, des cellules présentatrices d'antigènes tolérogènes (comme les cellules dendritiques) et des macrophages producteurs d'IL-10, qui fonctionnent tous pour supprimer les réponses inflammatoires. » – Nature, Cellular & Molecular Immunology[13]
Dans le contexte du diabète de type 1, le butyrate protège les cellules des îlots pancréatiques en réduisant la signalisation NF-κB et la production de cytokines inflammatoires. Des études montrent que les enfants atteints de ce diabète présentent des niveaux plus faibles d'acétate et de butyrate dans leurs selles[13]. Pour la polyarthrite rhumatoïde, le butyrate stimule les Bregs producteurs d'IL-10, réduisant ainsi l'inflammation articulaire[13].
Une recherche menée en 2022 par des scientifiques de la Sorbonne Université et de l'INSERM a révélé qu'un traitement par IL-2 à faible dose modifie la composition du microbiote intestinal, augmentant la production d'AGCC. Transférer ce microbiote modifié à des souris via une transplantation fécale a permis de protéger les souris contre la colite induite par DSS et de prévenir le diabète chez des souris NOD[6].
| Type d'AGCC | Récepteurs principaux | Effets anti-inflammatoires clés |
|---|---|---|
| Acétate (C2) | GPR43, GPR41 | Corrige les anomalies des cellules T ; AGCC le plus abondant dans le sang périphérique |
| Propionate (C3) | GPR43, GPR41 | Renforce l'activité des Tregs ; inhibe les réponses inflammatoires Th1 et Th17 |
| Butyrate (C4) | GPR109A, GPR43, PPARγ | Source d'énergie pour les colonocytes ; inhibe les HDAC ; induit IL-10 et TGF-β |
Cependant, tous les métabolites microbiens ne sont pas bénéfiques. Certains, comme le TMAO, favorisent des réponses inflammatoires.
TMAO et effets pro-inflammatoires
Contrairement aux AGCC, le triméthylamine-N-oxyde (TMAO) est un métabolite lié à des états inflammatoires, souvent produit en cas de dysbiose. Alors que les AGCC encouragent la tolérance immunitaire en stimulant les Tregs et les cytokines anti-inflammatoires comme l'IL-10, le TMAO active des lymphocytes autoréactifs et prolonge les réponses inflammatoires[13].
« Dans la dysbiose microbienne, des métabolites pathogènes, tels que certains dérivés d'acides biliaires, le formate, le triméthylamine-N-oxyde, les polyamines et le sulfure d'hydrogène, sont produits à la place des AGCC. Ces métabolites endommagent les tissus et augmentent les activités inflammatoires des cellules immunitaires. » – Nature, Cellular & Molecular Immunology[13]
Le TMAO compromet la tolérance immunitaire en augmentant la perméabilité intestinale, un phénomène souvent appelé leaky gut. Cela permet à des produits microbiens de pénétrer dans la circulation sanguine, déclenchant une inflammation systémique via l'activation des récepteurs Toll (TLR)[13][9]. Chez les patients atteints de lupus érythémateux systémique (LES), la dysbiose se manifeste fréquemment par un déséquilibre du ratio Firmicutes/Bacteroidetes, favorisant la production de métabolites inflammatoires comme le TMAO[1].
Cette opposition entre les AGCC bénéfiques et le TMAO inflammatoire met en lumière l'importance d'un microbiote équilibré pour prévenir les maladies auto-immunes et pourrait servir de base à de nouvelles approches pour améliorer la santé intestinale.
sbb-itb-044d621
Améliorer la santé intestinale pour réduire l'auto-immunité
Les recherches récentes montrent qu'il est possible d'agir sur le microbiote pour limiter les réactions auto-immunes. Voici des pistes nutritionnelles et des solutions naturelles pour rétablir l'équilibre microbien.
Fibres alimentaires et antioxydants
Les fibres alimentaires sont essentielles pour nourrir les bactéries bénéfiques de l’intestin. En consommant des fibres solubles et des glucides non digestibles, on favorise la croissance de bactéries comme les Lachnospiraceae, qui produisent des acides gras à chaîne courte (AGCC) tels que le butyrate, l’acétate et le propionate. Ces acides gras renforcent la barrière intestinale tout en réduisant l’inflammation[1][15].
Adopter un régime méditerranéen, riche en fibres et pauvre en viande rouge, peut nettement améliorer la diversité microbienne. Par exemple, l’étude FINRISK (2014-2021), menée sur 6 953 participants en Finlande, a révélé qu’une augmentation de Lactobacillus paracasei était associée à une pression artérielle plus basse et à une consommation réduite de sodium[15].
Les antioxydants jouent également un rôle clé en activant la voie Nrf2, un mécanisme qui aide à neutraliser les espèces réactives de l’oxygène (ROS). Ces molécules, souvent responsables de l’inflammation, peuvent ainsi être contrôlées.
« Le microbiome intestinal, en tant qu'intermédiaire entre certains effecteurs environnementaux externes et le système immunitaire, aide à programmer le système immunitaire pour qu'il soit tolérant aux antigènes externes innocents et aux auto-antigènes. » – Walaa Abdelaty Shaheen, Université de Birmingham[2]
En parallèle, réduire les aliments pro-inflammatoires peut renforcer ces bienfaits.
Réduire les graisses alimentaires et les aliments inflammatoires
Les régimes occidentaux, riches en viande rouge et en graisses saturées mais pauvres en fibres, favorisent la prolifération de bactéries pro-inflammatoires comme Bacteroides spp et Ruminococcus torques[1]. Ces bactéries affaiblissent la barrière intestinale, permettant aux lipopolysaccharides (LPS) de pénétrer dans le sang et de déclencher des réponses immunitaires[8].
Limiter les aliments ultra-transformés et les additifs alimentaires peut préserver la diversité microbienne. Réduire la consommation de graisses saturées aide aussi à freiner l’expansion des cellules Th17, souvent impliquées dans les inflammations articulaires et systémiques[1][14]. Ces ajustements nutritionnels protègent la barrière intestinale et limitent les réactions inflammatoires.
Pour aller plus loin, la supplémentation ciblée peut compléter ces efforts en agissant directement sur le microbiote.
Supplémentation naturelle pour la santé intestinale
Les probiotiques, prébiotiques et synbiotiques jouent un rôle crucial dans le rééquilibrage du microbiote et la modulation de la réponse immunitaire. Une étude sur 60 patients atteints de polyarthrite rhumatoïde a montré qu’une supplémentation de 8 semaines avec Lactobacillus casei, L. acidophilus et Bifidobacterium bifidum améliorait significativement le score d’activité de la maladie (DAS-28) et réduisait les niveaux de protéine C-réactive à haute sensibilité (hs-CRP)[2].
L’étude TEDDY (The Environmental Determinants of Diabetes in the Young), publiée en 2022, a suivi 8 676 enfants et constaté que l’administration de probiotiques dans les 27 premiers jours de vie réduisait l’incidence de l’auto-immunité des îlots pancréatiques[2].
Les prébiotiques, comme l’inuline et les oligofructoses, nourrissent les bactéries bénéfiques et renforcent la barrière intestinale[8][1]. Les synbiotiques, qui combinent probiotiques et prébiotiques, offrent des effets combinés pour réduire les inflammations coliques[8].
Purvival propose des compléments naturels validés scientifiquement pour soutenir la santé intestinale et l’équilibre immunitaire. Leurs produits, développés dans des laboratoires certifiés (GMP, ISO 22000), utilisent des ingrédients naturels à des dosages optimaux, sans OGM ni additifs artificiels. Ces suppléments s’intègrent facilement dans une stratégie globale pour prévenir les déséquilibres auto-immuns.
| Type de supplément | Fonction principale | Exemples de souches |
|---|---|---|
| Probiotiques | Microbes vivants bénéfiques qui soutiennent le système immunitaire et augmentent la diversité bactérienne | Lactobacillus casei, Bifidobacterium bifidum |
| Prébiotiques | Fibres non digestibles qui nourrissent les bactéries bénéfiques | Inuline, Oligofructose |
| Postbiotiques | Produits bioactifs issus du métabolisme bactérien, aux effets immunomodulateurs | Butyrate, Acétate, Propionate (AGCC) |
| Synbiotiques | Combinaisons de probiotiques et prébiotiques pour des effets synergiques | L. casei + Inuline |
Conclusion
Les recherches actuelles mettent en lumière un lien clair entre le microbiote intestinal et les maladies auto-immunes. La dysbiose, caractérisée par une diminution de la diversité microbienne, une altération de la barrière intestinale et un déséquilibre entre les cellules T régulatrices et pro-inflammatoires, joue un rôle central dans ces pathologies.
« La dysbiose ou le déséquilibre du microbiote intestinal a été de plus en plus identifié comme l'un des principaux facteurs environnementaux pouvant moduler les réponses immunitaires et contribuer au développement des maladies auto-immunes. » – Current Clinical Microbiology Reports [5]
Face à ces découvertes, les efforts thérapeutiques s'orientent vers des solutions visant à restaurer cet équilibre fragile. Par exemple, en août 2022, l'équipe de David Klatzmann de Sorbonne Université a démontré que des traitements par IL-2 à faible dose pouvaient non seulement influencer la composition du microbiote, mais aussi que la transplantation de microbiote fécal offrait une protection contre des affections comme la colite et le diabète [6]. Ces résultats renforcent l'idée que cibler le système immunitaire peut également contribuer à remodeler le microbiote dans une direction bénéfique.
L'avenir des traitements semble s'inscrire dans une approche personnalisée, intégrant génétique, alimentation et facteurs environnementaux. Parmi les pistes prometteuses, les postbiotiques tels que le butyrate ou encore les bactéries génétiquement modifiées suscitent un intérêt croissant [5][7].
« Le microbiome intestinal a une importance diagnostique potentielle pour prédire la progression de la maladie. » – Mohammad Adawi, Laniado MC, Ariel University [7]
Avec plus d'un milliard de personnes dans le monde affectées par des maladies auto-immunes [14], la compréhension et la modulation du microbiote intestinal représentent un défi crucial pour la santé publique. Les interventions nutritionnelles, associées à des compléments naturels ciblés, offrent des solutions accessibles pour restaurer l'équilibre microbien et soutenir la régulation du système immunitaire. Dans cette optique, des initiatives comme celles proposées par Purvival mettent à disposition des solutions naturelles basées sur des données scientifiques pour promouvoir une meilleure santé intestinale et immunitaire.
Sources
Les informations de cet article s'appuient sur des recherches scientifiques récentes et des revues systématiques validées par des comités de lecture. Voici les références utilisées pour explorer les liens entre le microbiote intestinal et les maladies auto-immunes :
- [1] Wang, X., et al. « Emerging role of gut microbiota in autoimmune diseases. » Frontiers in Immunology, mai 2024. doi:10.3389/fimmu.2024.1365554
- [5] « Gut Microbiota and Autoimmune Diseases: Mechanisms, Treatment, Challenges, and Future Recommendations. » Current Clinical Microbiology Reports
- [6] Tchitchek, N., et al. « Low-dose IL-2 shapes a tolerogenic gut microbiota that improves autoimmunity and gut inflammation. » JCI Insight, août 2022. doi:10.1172/jci.insight.159406
- [7] Adawi, M. « Meta-analysis of high-throughput sequencing data in immune-mediated diseases. » Frontiers in Microbiomes, mai 2025
- [12] Eberl, G. « Commensal microbiota influence systemic autoimmune responses. » The EMBO Journal
- [14] Données épidémiologiques sur l'incidence mondiale des maladies auto-immunes
- [16] « The composition of intestinal microbial communities plays a crucial role in maintaining immune homeostasis. » PubMed
FAQs
Comment diversifier mon microbiote intestinal pour réduire les risques de maladies auto-immunes ?
Pour maintenir un microbiote intestinal équilibré et diversifié, il est crucial de prêter attention à son alimentation et à son mode de vie. Consommer des aliments riches en fibres, comme les légumineuses, les céréales complètes, les fruits et les légumes, est un excellent point de départ. Les aliments fermentés, tels que le yaourt, le kéfir, la choucroute ou le miso, jouent également un rôle important en nourrissant les bactéries bénéfiques et en limitant les déséquilibres microbiens. À l'inverse, il est préférable de réduire la consommation de sucres raffinés, de graisses saturées et d'additifs alimentaires, qui peuvent favoriser la prolifération de bactéries nuisibles.
L'usage d'antibiotiques doit être limité aux situations médicalement nécessaires, car ces médicaments, bien qu'importants, peuvent temporairement réduire la diversité des micro-organismes intestinaux. Pour renforcer cette diversité, vous pouvez envisager des compléments de probiotiques et de prébiotiques de qualité. Par exemple, les produits de Purvival offrent des souches soigneusement sélectionnées et des fibres prébiotiques qui soutiennent efficacement la flore intestinale.
Enfin, n'oubliez pas que votre mode de vie a un impact direct sur votre microbiote. Une activité physique régulière, une gestion efficace du stress et un sommeil réparateur (idéalement entre 7 et 9 heures par nuit) favorisent une interaction optimale entre votre microbiote et votre système immunitaire. Ce lien contribue à une meilleure protection contre certaines maladies, notamment auto-immunes.
Comment les acides gras à chaîne courte influencent-ils l’inflammation et les maladies auto-immunes ?
Les acides gras à chaîne courte (AGCC), tels que l’acétate, le propionate et le butyrate, sont générés dans l’intestin grâce à la fermentation des fibres alimentaires. Ces composés jouent un rôle essentiel dans la modulation de l’inflammation en interagissant avec des récepteurs spécifiques présents sur les cellules immunitaires. Cette interaction contribue à plusieurs mécanismes bénéfiques : elle renforce la barrière intestinale, limite la production de cytokines pro-inflammatoires comme l’IL-6 et le TNF-α, et favorise la libération de cytokines aux propriétés anti-inflammatoires, telles que l’IL-10.
Ces actions participent au maintien d’un équilibre immunitaire et pourraient aider à prévenir certaines maladies auto-immunes. Cependant, il est important de noter que leur impact peut varier en fonction des concentrations et des contextes spécifiques, certains AGCC pouvant, dans certaines conditions, amplifier des réponses inflammatoires. Une alimentation riche en fibres, ainsi que l’utilisation de compléments alimentaires ciblés, constitue une approche intéressante pour stimuler leur production. En soutenant la santé du microbiote, ces stratégies pourraient contribuer à limiter les désordres inflammatoires. Les solutions naturelles proposées par Purvival visent précisément à encourager cet équilibre pour promouvoir un bien-être global.
Quel rôle joue le microbiote intestinal dans le développement des maladies auto-immunes ?
Le microbiote intestinal joue un rôle clé dans le bon fonctionnement de notre système immunitaire. Mais lorsqu’il est déséquilibré, une situation appelée dysbiose, les conséquences peuvent être profondes. Ce déséquilibre fragilise la barrière intestinale, laissant passer des molécules pro-inflammatoires dans la circulation sanguine. Résultat : les mécanismes de régulation immunitaire sont perturbés, ce qui peut déclencher une réponse inflammatoire excessive et une perte de tolérance immunitaire. Ces dérèglements sont souvent associés à l’apparition ou à l’aggravation de maladies auto-immunes comme le diabète de type 1, la polyarthrite rhumatoïde ou encore la sclérose en plaques.
Les avancées scientifiques récentes établissent également un lien entre la dysbiose, l’inflammation chronique et l’activation de cellules immunitaires auto-réactives. Face à ces constats, rétablir un équilibre dans le microbiote intestinal apparaît comme une solution prometteuse pour limiter ces risques. Parmi les approches naturelles, certains compléments alimentaires de qualité peuvent favoriser une diversité microbienne saine et aider à réduire l’inflammation liée aux maladies auto-immunes. Ces pistes, bien que encourageantes, nécessitent souvent un accompagnement personnalisé pour maximiser leurs bénéfices.